مقالات
آشنایی با باتری ماشین
باتری 12 ولت سرب اسید ماشین. این باتری های بزرگ و نسبتا سنگین در هر وسیله نقلیه موتور احتراقی استفاده می شود. آنها جزء ضروری خودرو هستند. بنابراین چه کاری انجام می دهد و چگونه کار می کند؟ این چیزی است که ما در این مقاله درباره آن صحبت می کنیم.
باتری ماشین چیست؟
باتری 12 ولتی ماشین چیزی شبیه به این است.
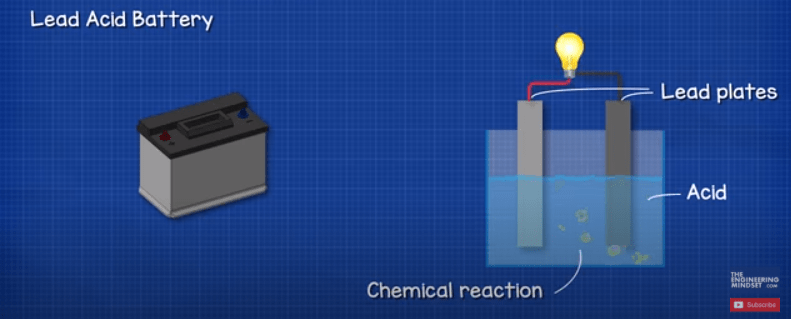
ما آن را باتری اسید سرب می نامیم زیرا در داخل واحد صفحات سربی وجود دارد که در اسید غوطه ور می شوند. این یک واکنش شیمیایی ایجاد می کند که انرژی آزاد می کند و ولتاژ و جریان را برای ما فراهم می کند.
واکنش شیمیایی درون باتری ماشین
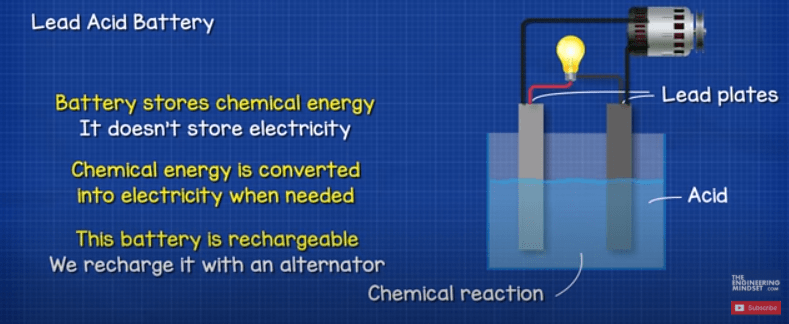
بنابراین باتری انرژی را به شکل انرژی شیمیایی ذخیره می کند. برق را ذخیره نمی کند این انرژی شیمیایی هر زمان که به آن نیاز داشته باشیم به انرژی الکتریکی تبدیل می شود. این باتری همچنین قابل شارژ است، اگر باتری را با برق تامین کنیم، می توانیم واکنش شیمیایی را معکوس کنیم و باتری را دوباره شارژ کنیم.
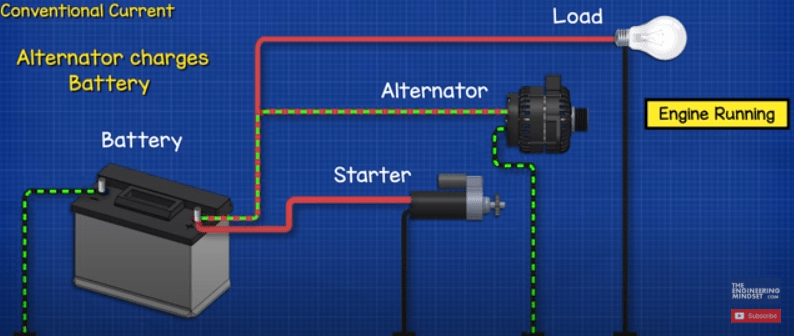
شارژ باتری ماشین با دینام
این نوع باتری ها می توانند مقدار زیادی جریان را به خصوص در مقایسه با باتری های معمولی، کوچکتر و قلیایی خانگی ارائه دهند.
چرا از باتری در خودرو استفاده می شود؟
باتری معمولی خودرو در قسمت موتور خودرو قرار دارد. باتری ابتدا برای راه اندازی موتور مورد استفاده قرار می گیرد و این کار را با تامین برق یک موتور الکتریکی کوچک به نام موتور استارت انجام می دهد. همچنین برای شروع احتراق سوخت، برق را به سیستم جرقه زنی می دهد.
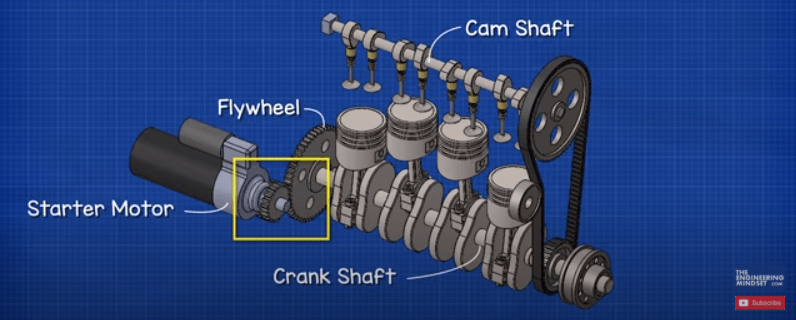
استارت موتور
موتور استارت یک دنده کوچک را روی فلایویل موتور درگیر می کند. این کار را انجام می دهد تا میل لنگ را بچرخاند که موتور احتراقی را روشن می کند، دنده کوچک سپس جدا می شود و موتور خود به خود کار می کند. موتور استارتر برای اینکه بتواند فلایویل را بچرخاند به نیروی زیادی نیاز دارد، بنابراین موتور استارت یک جریان بسیار زیاد، احتمالاً صدها آمپر، فقط برای چند ثانیه می کشد. این جریان زیاد انرژی ذخیره شده در باتری را کاهش می دهد. بنابراین ما باید آن را پشتیبان گیری کنیم.
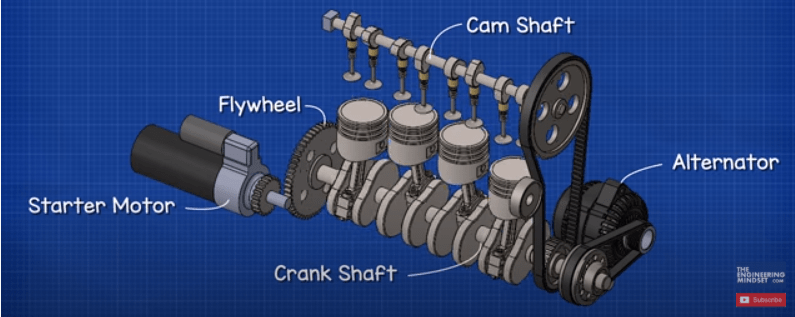
دینام
یک دینام به موتور متصل است. دینام توسط موتور می چرخد و با چرخش آن برق تولید می کند. این برای شارژ مجدد به باتری بازگردانده می شود.
در حالی که موتور در حال کار است، دینام باتری را شارژ می کند، اما انرژی الکتریکی مواردی مانند سیستم روشنایی و موسیقی را نیز تامین می کند. زمانی که تقاضا برای الکتریسیته بیشتر از چیزی باشد که دینام می تواند تامین کند، باتری نیروی اضافی را تامین می کند که دوباره باتری را تخلیه می کند.
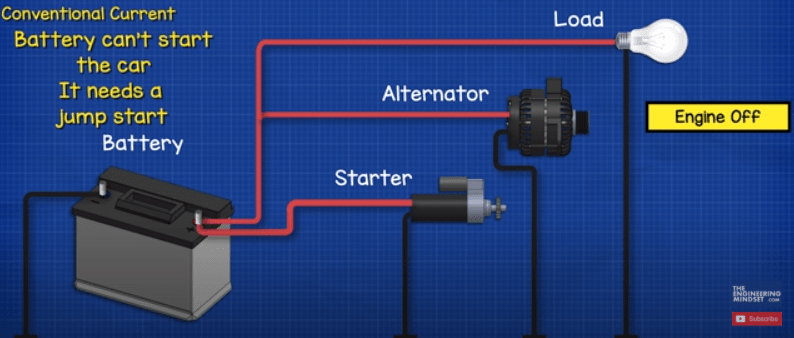
اگر موتور خاموش باشد، دینام چرخش و شارژ مجدد باتری را متوقف می کند، بنابراین باتری تا زمانی که تمام شود، برق کامل را تامین می کند. در این مرحله باتری نمی تواند الکتریسیته کافی برای روشن کردن موتور را تامین کند، بنابراین باید ماشین را به سرعت روشن کنیم.
قسمت های اصلی سیستم برق ماشین
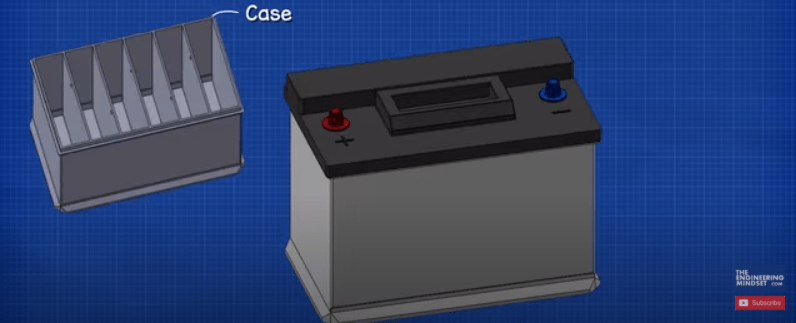
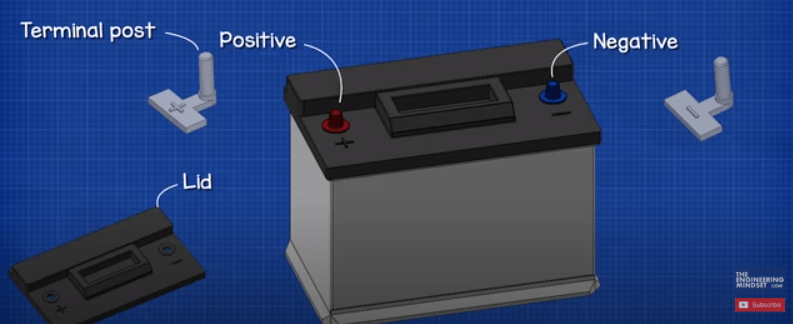
بیایید نگاهی به اجزای اصلی باتری ماشین بیندازیم و سپس نحوه عملکرد آن را توضیح می دهیم. اول از همه، ما یک قاب پلاستیکی داریم که تمام اجزای داخلی را در جای خود نگه می دارد. در قسمت بالایی درپوش پلاستیکی داریم و دو ترمینال مثبت و منفی وجود دارد که به آنها پایه ترمینال می گویند.
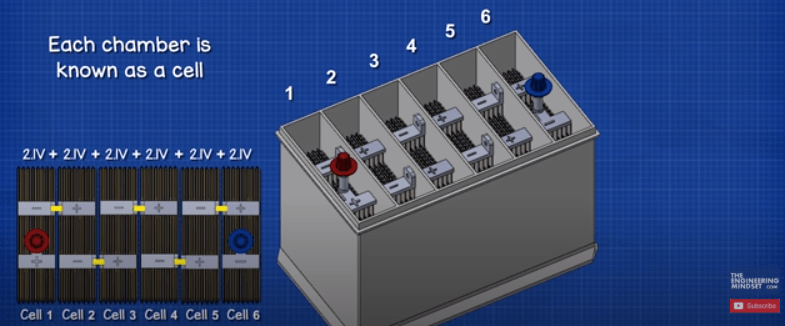
با برداشتن درب داخل آن را می بینیم. توجه داشته باشید که پوشش به 6 محفظه مجزا تقسیم شده است که هر کدام با یک دیوار پلاستیکی از هم جدا شده اند. هر اتاقک به عنوان یک سلول شناخته می شود. هر سلول حدود 2.1 ولت DC یا جریان مستقیم تولید می کند. هر سلول به صورت سری وصل می شود، منفی یک سلول به مثبت سلول بعدی متصل می شود تا ولتاژ کل حدود 12.6 ولت به ما بدهد.
6 اتاق مجزا
مثل این است که اگر باتریهای قلیایی خانگی را به هم وصل کنید، ولتاژ آنها با هم جمع میشوند تا ولتاژ کل بالاتری را ایجاد کنند.
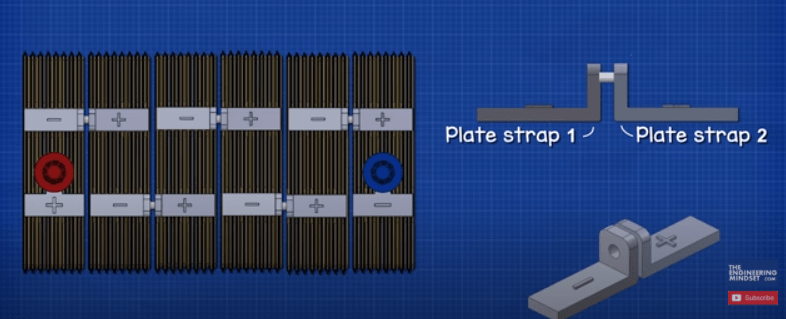
هر سلول در باتری از طریق بند صفحه ای که از سرب ساخته شده است به هم متصل می شود. اینها از طریق دیواره پلاستیکی به یکدیگر جوش داده می شوند تا اتصال را تشکیل دهند.
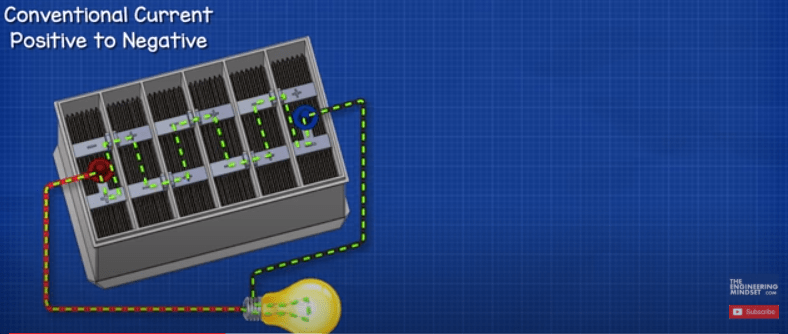
همانطور که از این منظر به باتری نگاه می کنیم، می بینیم که جریان از طریق سلول های باتری از مثبت به منفی می گذرد و این با استفاده از نظریه جریان معمولی است. آنچه در واقع اتفاق می افتد این است که الکترون ها در جهت مخالف از منفی به مثبت جریان می یابند. اما کمی بعد در مقاله به آن خواهیم پرداخت.
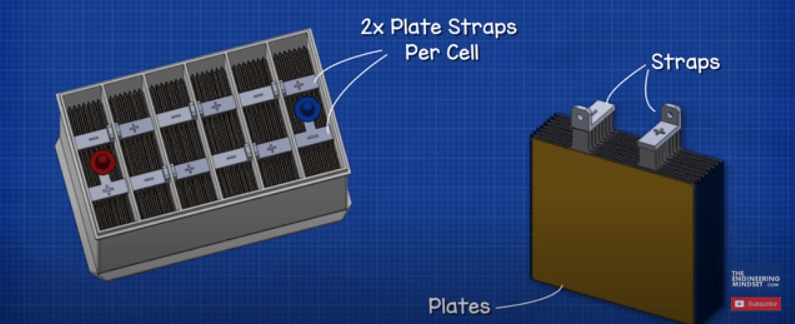
توجه داشته باشید که در هر سلول دو بند صفحه وجود دارد. یکی مثبت و یکی منفی. به این تسمه های صفحه ای می گویند زیرا هر تسمه به تعدادی صفحه که ورقه های سربی هستند متصل است.
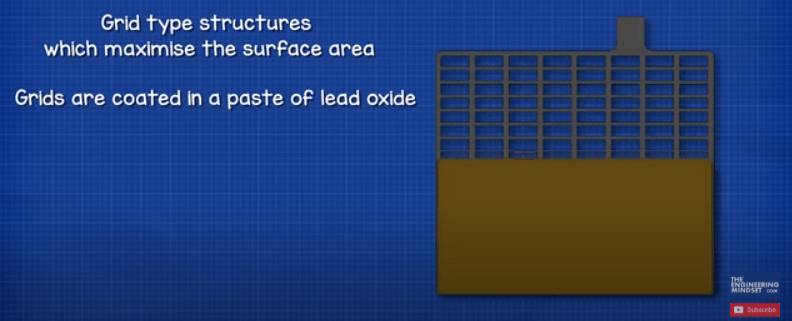
صفحات به ساختارهای شبکه ای تبدیل می شوند که سطح را به حداکثر می رساند. شبکه ها در خمیر اکسید سرب پوشانده شده اند. خمیر جایی است که واکنش شیمیایی رخ می دهد و کمی بعد در مقاله خواهیم دید. خمیر کمی مانند یک اسفنج عمل می کند و مقداری از مایع الکترولیت را جذب می کند که عملکرد باتری را بهبود می بخشد. اندازه صفحه تعیین میکند که باتری چقدر جریان دارد، اما ولتاژ را تغییر نمیدهد. مواد مورد استفاده و تعداد صفحات تعیین کننده ولتاژ تولید شده توسط هر سلول است. شبکه خمیر را در جای خود نگه می دارد تا از توزیع یکنواخت جریان در سراسر صفحه اطمینان حاصل کند و به انتقال الکترون ها به خارج از باتری و اطراف مدار الکتریکی کمک می کند.
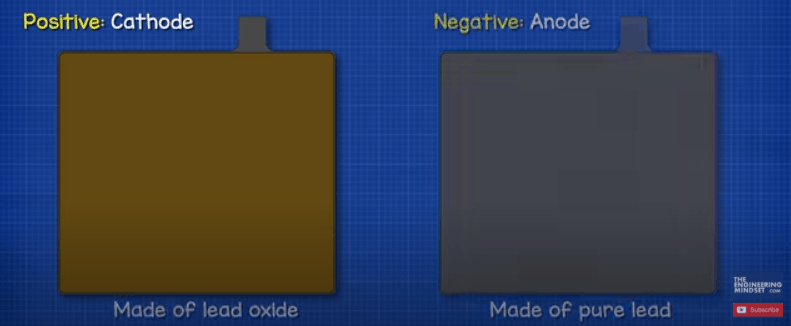
صفحه منفی آند است و این صفحه ای از سرب خالص است، اگرچه مقادیر کمی از مواد افزودنی برای سفت شدن سرب و محافظت از آن در برابر خوردگی اضافه می شود. صفحه مثبت کاتد است و از اکسید سرب ساخته شده است. صفحات از مواد غیر مشابه برای تشکیل واکنش شیمیایی و آزاد کردن الکترون ساخته شده اند. ما نمی خواهیم صفحات مثبت و منفی با یکدیگر تماس پیدا کنند، این باعث اتصال کوتاه باتری می شود. بنابراین، در عوض، هر صفحه مثبت را در یک جداکننده پاکت قرار می دهیم. این یک ماده متخلخل است که به یون ها اجازه می دهد بدون تماس مستقیم مواد با یکدیگر جریان پیدا کنند.
صفحه مثبت باتری
صفحات مثبت و منفی با یک شکاف کوچک در بین یکدیگر قرار می گیرند. سپس محفظه با مایع الکترولیت اسید سولفوریک و آب پر می شود. از این رو باتری را باتری اسید سرب می نامند.
اصول برق باتری
ما میخواهیم بهسرعت اصول الکتریسیته را مرور کنیم تا قسمت بعدی نحوه کار باتری را درک کنید.
الکترون های باتری
الکتریسیته جریان الکترون ها در مدار است. ما به تعداد زیادی الکترون نیاز داریم که در یک جهت در یک سیم جریان پیدا کنند تا بتوانیم چیزهایی مانند لامپ ها را در مسیر حرکت الکترون ها قرار دهیم. الکترون ها باید از این طریق عبور کنند و در حین انجام نور تولید می کنند. هنگامی که تعداد زیادی الکترون در یک جهت جریان دارند، این جریان را خوب صدا کنید.
اتم ها
هر ماده ای از اتم ساخته شده است. اتم ها دارای تعداد پروتون، نوترون و الکترون متفاوتی هستند که این چیزی است که ماده را متفاوت می کند. برخی از مواد مانند مس دارای الکترونی هستند که آزادانه به اتم های دیگر حرکت می کند. اگر منبع تغذیه ای مانند باتری را به سیم مسی وصل کنیم، ولتاژ الکترون ها را فشار می دهد و آنها برای رسیدن به پایانه مثبت باتری عجله می کنند.
گفتیم که الکترون ها از منفی به مثبت جریان می یابند. این به عنوان جریان الکترون شناخته می شود، این یک نظریه است که چگونه الکتریسیته کار می کند و این چیزی است که در واقع اتفاق می افتد. اما، ممکن است به دیدن جریان معمولی که از مثبت به منفی است عادت کرده باشید، این نظریه اصلی است که به عنوان جریان معمولی شناخته می شود. این اشتباه توسط جوزف تامپسون ثابت شد که الکترون را کشف کرد و دریافت که آنها از منفی به مثبت جریان می یابند.
با این حال، ما هنوز تا به امروز از تئوری جریان معمولی هنگام طراحی مدارهای الکتریکی استفاده می کنیم. اگر به این مدار ساده نگاه کنیم، همیشه باید فرض کنیم که جریان از مثبت به منفی در جریان است، اما مهندسان و دانشمندان می دانند که الکترون ها در واقع در جهت مخالف جریان دارند. فرمولهای الکتریکی که ما استفاده میکنیم بدون توجه به اینکه برق از کدام طرف جریان دارد، همچنان با همان پاسخها ظاهر میشوند، بنابراین واقعاً مهم نیست.
جریان DC
دو نوع برق وجود دارد، جریان مستقیم DC که ما از باتری ها دریافت می کنیم. الکترون های این نوع در یک جهت رانده می شوند. بنابراین جریان مستقیم نامیده می شود. نوع دیگر برق AC یا جریان متناوب است که از پریزهای برق خانه خود دریافت می کنید. در این نوع الکترون ها به طور مداوم به جلو و عقب رانده و کشیده می شوند. به این نوع فکر کنید مانند جزر و مد دریا که در داخل و خارج جریان دارد.
جریان متناوب
وقتی مواد خاصی را با هم مخلوط می کنیم، می توانیم واکنش های شیمیایی ایجاد کنیم. این زمانی است که اتم های یک ماده با اتم های یک ماده دیگر برهم کنش می کنند. در طی این برهمکنش اتم ها به یکدیگر پیوند می خورند یا از هم جدا می شوند. الکترون ها همچنین می توانند توسط اتم ها در طی واکنش آزاد یا جذب شوند.
واکنش شیمیایی
وقتی در مورد اتم صحبت می کنیم، معمولاً اصطلاح یون استفاده می شود. یون اتمی است که دارای تعداد پروتون یا الکترون نامساوی است. وقتی اتم دارای تعداد پروتون و الکترون یکسان باشد، تغییر خنثی دارد، زیرا پروتونها تغییر مثبت میکنند و الکترونها بار منفی دارند، بنابراین متعادل میشوند. اگر اتم الکترون بیشتری نسبت به پروتون داشته باشد، یک یون منفی است. اگر پروتون اتم بیشتر از الکترون باشد، یون مثبت است.
باتری ماشین چگونه کار می کند
به جای تلاش برای درک این ساختار پیچیده، ما آن را به این مدل ساده از یک سلول با یک کاتد و آند ساده میکنیم.
در این سلول ما مایع الکترولیت داریم که 1/3 اسید سولفوریک و 2/3 آب است.
ما یک الکترود مثبت داریم که کاتد است، این الکترود از اکسید سرب (PbO2) ساخته شده است.
سپس الکترود مثبت را داریم که آند است، این الکترود از سرب خالص (Pb) ساخته شده است.
کاتد و آند
وقتی این مواد با هم ترکیب می شوند، یک واکنش شیمیایی کوچک بین اتم ها ایجاد می کنیم. ما اتم های این مواد را با این کره های رنگی نشان خواهیم داد.
پایانه کاتد مثبت اکسید سرب (PbO2) با سولفات (SO4-2) در الکترولیت واکنش می دهد، این یک لایه از سولفات سرب (PbSO4) روی پایانه کاتد تشکیل می دهد. در طی این واکنش، یک یون اکسیژن (O2-2) از کاتد به داخل الکترولیت خارج می شود. هنگامی که در الکترولیت قرار می گیرند، این یون های اکسیژن با یون های هیدروژن (H+) ترکیب می شوند و آب (H2O) را تشکیل می دهند.
در همان زمان، اتمهای سرب روی آند با یونهای سولفات (SO4-2) در الکترولیت واکنش میدهند. این واکنش باعث ایجاد لایه ای از سولفات سرب (PbSO4) در اطراف الکترود می شود. در طی این واکنش دو الکترون آزاد می شوند و در ترمینال منفی جمع می شوند.
بنابراین اکنون ما یک تجمع الکترون در ترمینال منفی داریم. از آنجایی که الکترون ها دارای بار منفی هستند، به این معنی است که ما در دو پایانه بار اختلاف داریم و می توانیم آن را با یک ولت متر یا مولتی متر اندازه گیری کنیم.
اگر به یک آهنربا فکر کنید، دو طرف مقابل جذب می شوند و انتهای یکسان یکدیگر را دفع می کنند. الکترون ها دارای بار منفی هستند و بنابراین یکدیگر را دفع می کنند و به سمت ترمینال مثبت که الکترون کمتری دارد جذب می شوند. اما، آنها نمی توانند به این برسند. اگر برای الکترونها مسیری مانند سیم فراهم کنیم، الکترونها از این مسیر عبور میکنند تا به پایانه مثبت برسند. سپس میتوانیم چیزهایی مانند لامپ را در مسیر این الکترونها قرار دهیم و از آنها برای انجام کارهایی مانند روشن کردن لامپ استفاده کنیم.
در حالی که مسیر وجود دارد، واکنش شیمیایی ادامه می یابد، اما این تا ابد ادامه نخواهد داشت. مواد شیمیایی مورد نیاز برای واکنش تمام می شود. اسید رقیقتر و ضعیفتر میشود و تجمع سولفات سرب هر دو الکترود را میپوشاند، به این معنی که مواد شبیهتر میشوند و بنابراین دستیابی به واکنش شیمیایی سختتر میشود.
اما خوشبختانه این واکنش شیمیایی را می توان معکوس کرد، بنابراین اگر برق باتری را از دینام تامین کنیم، می توانیم واکنش را معکوس کنیم.
می تواند واکنش را معکوس کند
الکترون ها وارد ترمینال منفی می شوند و دوباره به سولفات سرب می پیوندند و سولفات را در الکترولیت رها می کنند تا فقط سرب روی صفحه منفی باقی بماند. یونهای سوفلات وارد الکترولیت میشوند و با یون هیدروژن ترکیب میشوند تا یون اکسیژن آزاد شود تا اسید الکترولیت قویتر شود. یون اکسیژن با سرب ترکیب می شود و اکسید سرب ایجاد می کند و این سوفلات را دوباره به الکترولیت آزاد می کند و دوباره آن را قوی تر می کند.
اگر بخواهیم باتری را برای مدت طولانی یا چند بار رها کنیم تا کاملاً تخلیه شود، معکوس کردن واکنش شیمیایی بسیار دشوار می شود. علاوه بر این، لایه سولفات می تواند از الکترودها جدا شود و در پایین باتری عادت کند که به این معنی است که دیگر در واکنش شیمیایی شرکت نمی کند بنابراین باتری نیاز به تعمیر یا تعویض دارد.
بنابراین وقتی به باتری نگاه میکنیم، این واکنش شیمیایی بین هر صفحه در هر سلول رخ میدهد تا صدها آمپر جریان برای راهاندازی موتور استارت و همچنین تامین ولتاژ برای تغذیه چراغها و غیره فراهم کند. سپس این ولتاژ توسط دینام شارژ میشود.
تست باتری ماشین با مولتی متر
برای آزمایش ولتاژ باتری ماشین، کافیست روی مولتی متر خود به تنظیم ولتاژ DC تغییر دهید و سپس سرب قرمز را به مثبت و سیم سیاه را به منفی وصل کنید. اگر ولتاژ زیر 12 باشد، باید ولتاژی در حدود 12.6 ولت ببینیم، پس باتری به درستی کار نمی کند.
موتور خاموش
هنگامی که ماشین را روشن می کنیم، ولتاژ کاهش می یابد زیرا موتور استارت مقدار زیادی جریان را می کشد. ولتاژ به حدود 11 ولت کاهش می یابد، اگر کمتر از حدود 10 ولت باشد، باتری به درستی کار نمی کند.
راه اندازی موتور
هنگامی که موتور کار می کند، دینام باید برق تولید کند و بنابراین باید شاهد ولتاژ بالاتری در حدود 14 ولت باشیم، زیرا دینام در حال شارژ مجدد باتری است و ولتاژ باید بالاتر باشد تا به عقب راندن الکترون ها و معکوس کردن مواد شیمیایی کمک کند.